
ExCell Bio News
近日,依科赛战略合作伙伴博生吉医药集团开发的UTAA09注射液临床试验申请已获得国家药监局受理。据悉,这是国内首个获得CDE受理的现货通用型UCAR-Vδ1T细胞疗法(UTAA09注射液)。依科赛对合作伙伴的这一重要进展表示热烈祝贺,倍感荣幸能够助力UTAA09注射液的进展,为此项目提供了免疫细胞无血清培养基产品和技术服务。
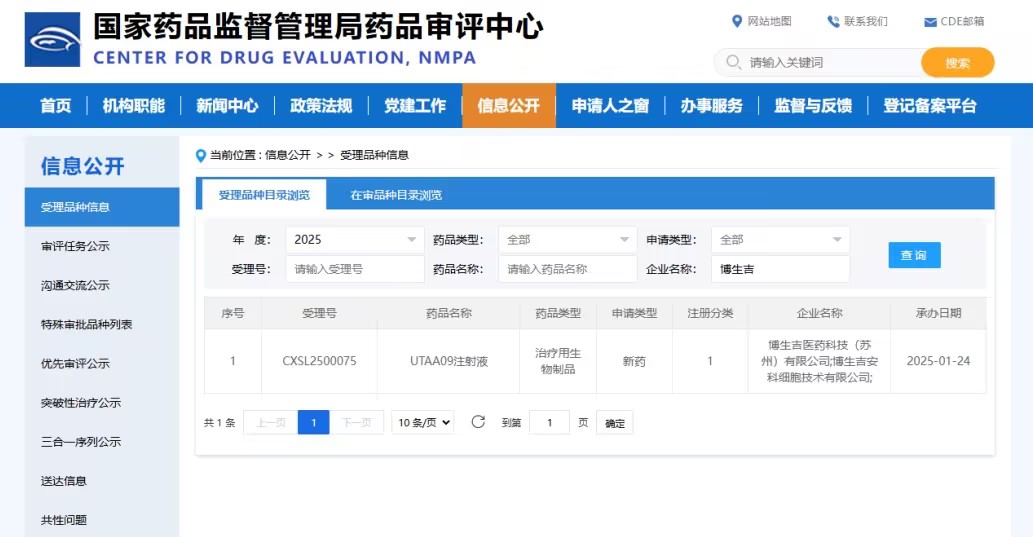
UTAA09注射液
UTAA09注射液是博生吉申报的首个通用现货型的CAR-T细胞产品,该产品是以健康供者单采血为起始原材料制备而成的UCAR-Vδ1T细胞产品。本次获得受理的UTAA09注射液,不仅保持了其强大的组织脏器归巢能力、而且在CMC制备工艺上,走在了全球前列,实现了细胞药物成本的极大改善,为UTAA09注射液未来将适应症拓展至自身免疫性疾病等适应症创造了条件。
依科赛在此衷心祝贺博生吉取得的新成就,并期待博生吉更多细胞治疗药物进展顺利,早日上市,惠及患者。依科赛多款无血清培养基(T/NK/293/CHO等) 已完成美国FDA DMF备案,并助力多家客户FDA/CDE申报,覆盖TCR-T、TIL、γδ-T、Car-T、UCAR-T及通用性NK细胞等多条技术管线,这也证明依科赛的生产工艺和品质控制体系已经达到了国际标准和监管要求,我们将继续秉持着“加快生命科技应用,造福百姓健康”的使命坚持为全球合作伙伴,提供高质量、高效的全方位产品服务,助推生物医药产业蓬勃发展。
依科赛无血清培养基
CGT GMP级无血清培养基首选品牌
01
合规稳定:
GMP级别,FDA备案,支持从研发到商业化,赋能生物药快速申报。
02
国际品质:
性能卓越,质量稳定,自研自产,数字化工厂,年产能达千万升。
03
多品类覆盖:
T/NK/293/MSC/CHO/冻液等产品线,全面覆盖CGT、生物制药领域。
04
定制化服务:
满足不同项目个性化需求(配方优化、包装定制等),实现降本增效。

关于博生吉医药
博生吉医药科技(苏州)有限公司于2010年5月31日注册成立在苏州工业园区。博生吉,PersonGen,Personalized Gene Therapy的缩写,寓意着致力于个性化医药技术的研发与创新,是杨林博士领衔、由一批在海外顶尖癌症临床治疗与研究机构工作10余年的生物医药专家携手创办的、以突破性肿瘤细胞免疫治疗技术与产品研发为主要发展目标的高科技企业。博生吉集团旗下全资子公司-博生吉安科细胞技术有限公司自2016年11月17日注册成立于安徽省合肥市高新区。自成立之日起,博生吉安科已经完成建筑面积10000平方米的硬件建设,包括可以达到国际一流水平的免疫细胞GMP制备车间、质粒与慢病毒GMP生产与纯化车间、P2安全实验室以及装备先进的质量控制实验室与研发实验室。拥有完整的从质粒、慢病毒、一直到CAR-T细胞制备的全链条生产体系。博生吉安科是我国到目前为止建设有完备的、国际领先的全自动、全密闭CAR-T细胞生产线的企业。
关于依科赛生物
依科赛生物(ExCell Bio)创立于2013年,以“加快生命科技应用,造福百姓健康”为使命,致力于解决生物医药卡脖子、实现关键原料国产化,现已成为中国生物医药上游核心原材料的领军企业之一。公司是是国家高新技术企业,国家级专精特新小巨人企业、国家知识产权优势企业、省和苏州市独角兽培育企业、中国首家国际血清行业协会(ISIA)会员单位,江苏省生物制药、细胞治疗等领域用CD无血清培养基工程研究中心。
公司当前聚焦无血清培养基、胎牛血清和鉴定试剂等三大产品板块,为生物药、细胞与基因治疗、基础科学研究客户提供国际品质的产品与服务。公司依托国际化和专业化的研发技术团队、质量和生产团队以及商业化团队,持续创新,追求卓越,在不断优化产品性能的同时,确保可靠的质量和稳定的供应,全面赋能生物医药产业的快速健康发展,打造细胞培养“中国芯”产品。


